Chirurgie guidée par fluorescence

POINTS CLÉS

Introduction
Depuis une décennie, les avancées technologiques transforment profondément la pratique chirurgicale vétérinaire. Si l’imagerie en coupe (IRM, scanner) a affiné le diagnostic et la planification préopératoire, la véritable révolution s’opère désormais *au cœur même de l’acte opératoire*. Parmi ces innovations, la chirurgie guidée par fluorescence s’impose comme un jalon décisif, permettant une visualisation en temps réel de structures anatomiques invisibles à l’œil nu.
Reposant sur l'utilisation de traceurs fluorescents, en particulier **l’indocyanine verte (ICG)**, cette technique combine les bénéfices de la mini-invasive et de l’imagerie dynamique, optimisant la sécurité, la précision et l’efficacité des gestes chirurgicaux. Elle trouve aujourd’hui des applications multiples en médecine vétérinaire : oncologie, chirurgie hépatobiliaire, reconstructrice, et thoracique.
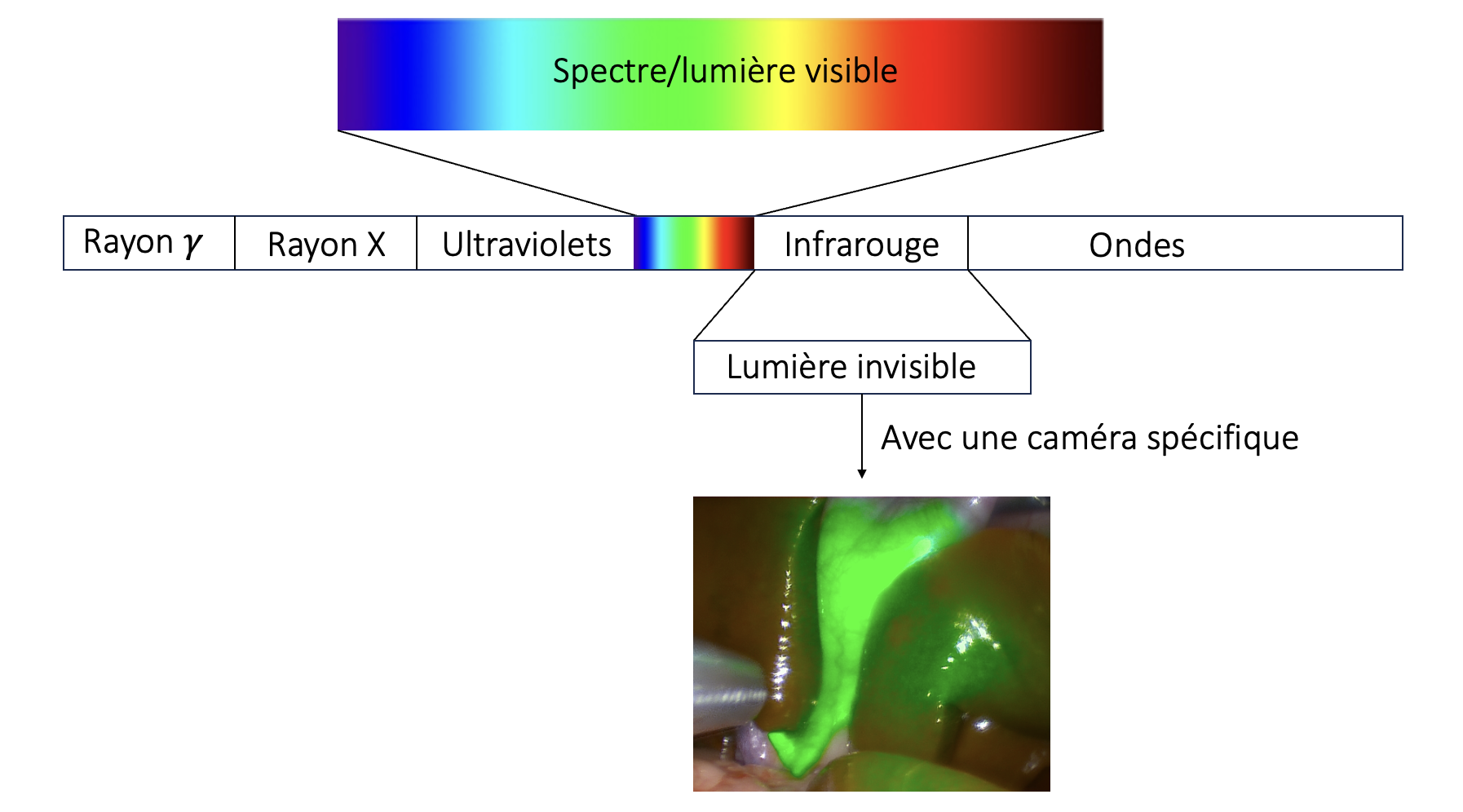
La chirurgie guidée par fluorescence repose sur un mécanisme relativement simple, mais redoutablement efficace. Après injection intraveineuse ou locale, l’indocyanine verte — un fluorophore hydrosoluble lié aux protéines plasmatiques — émet une fluorescence lorsqu’elle est excitée par une lumière proche infrarouge (800 nm). Cette émission est captée par des caméras spécifiques, souvent couplées à l’imagerie en lumière blanche, permettant une visualisation superposée des structures.
Particulièrement bien tolérée, éliminée rapidement par voie hépatique et excrétée dans la bile, l’ICG possède une faible toxicité et autorise des réinjections peropératoires, offrant ainsi une grande flexibilité opératoire. Ses propriétés physicochimiques lui confèrent une haute affinité pour le système vasculaire et lymphatique, d’où ses nombreuses applications.
Cartographie des nœuds lymphatiques sentinelles : une stratégie oncologique de précision
Dans la prise en charge chirurgicale des tumeurs, l’identification du nœud lymphatique sentinelle (NLS) est cruciale. Ce ganglion est le premier site de drainage lymphatique d’une tumeur, et donc potentiellement le premier foyer métastatique. La technique du "sentinel lymph node mapping" assistée par ICG permet de tracer le chemin lymphatique par injection intradermique péri-tumorale.
Chez le chien, les NLS sont visibles en quelques minutes grâce à l’imagerie infrarouge. Cette précision réduit la dissection, diminue les risques de lésions vasculaires ou nerveuses et évite la morbidité associée à des curages lymphatiques extensifs. L’ICG s’avère ici un véritable "guide lumineux" pour le chirurgien, renforçant la fiabilité de la stadification tumorale.

Injection péritumorale d’indocyanine verte visualisé à l’aide du laparoscope Arthrex Vet System®
Visualisation du nœud lymphatique sentinelle par laparoscopie

Visualisation des voies biliaires après injection d’ICG en image superposée par laparoscopie Arthrex Vet System®
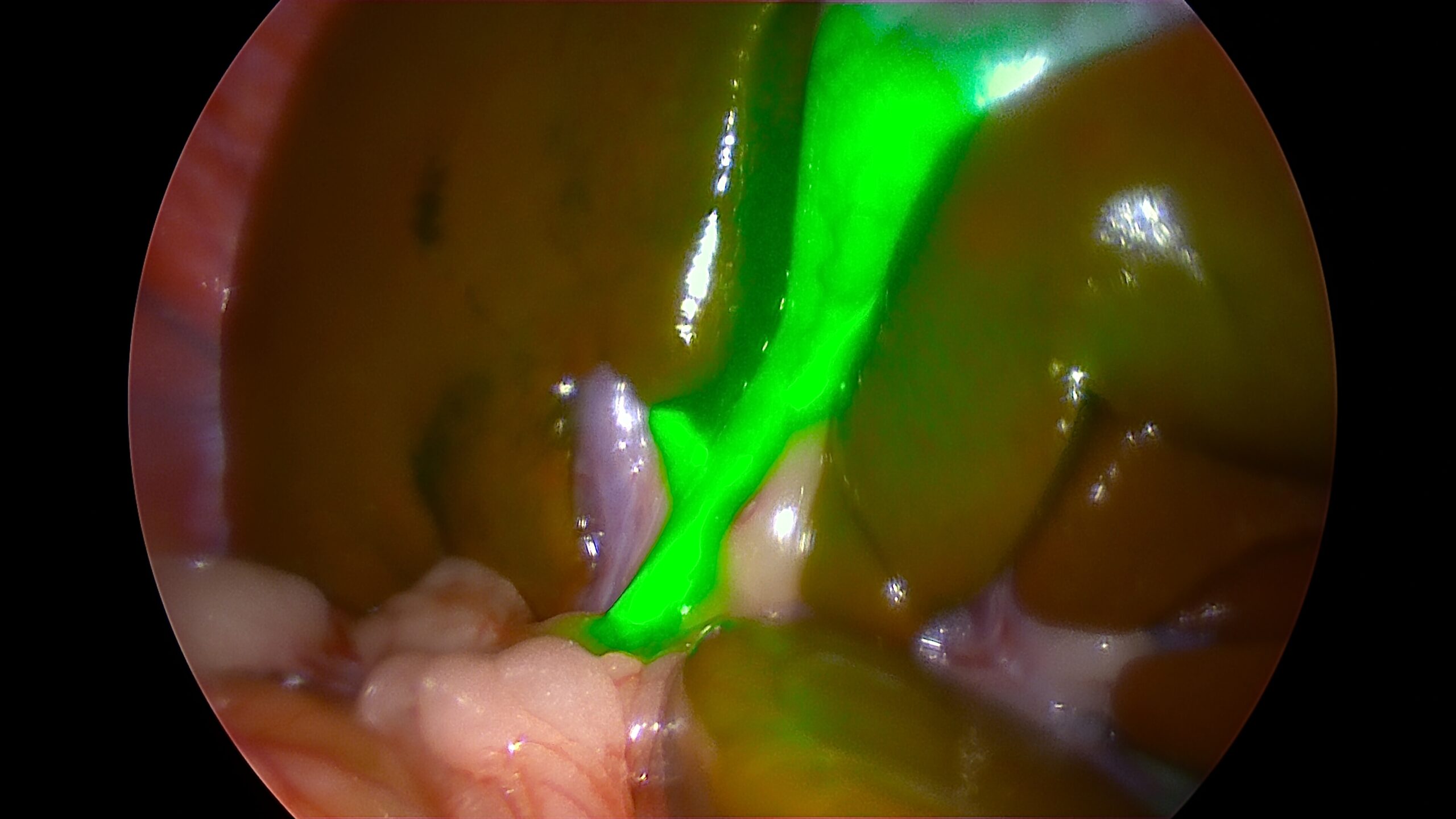
Cholécystectomie laparoscopique : une meilleure visualisation des voies biliaires
En chirurgie hépatobiliaire, notamment dans le traitement des mucocèles ou cholélithiases canines, la variabilité anatomique des voies biliaires extra-hépatiques peut compromettre la sécurité opératoire. En laparoscopie, cette difficulté est exacerbée par l’absence de rétroaction tactile.
L’injection d’ICG permet une cholangiographie dynamique : captée par les hépatocytes et excrétée dans la bile, la substance rend visible les voies biliaires à la caméra infrarouge, même à travers la graisse mésentérique. Des études cliniques montrent une réduction des lésions iatrogènes, du temps opératoire et des conversions en chirurgie ouverte. En chirurgie vétérinaire, cette approche trouve progressivement sa place, bien que des ajustements de dosage et de timing d’injection restent nécessaires.
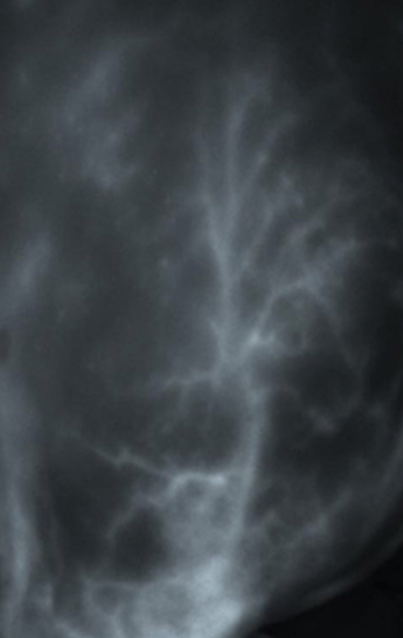
Visualisation de l’artère brachiale lors de réalisation d’un lambeau axial.
Évaluation de la perfusion cutanée en chirurgie reconstructrice
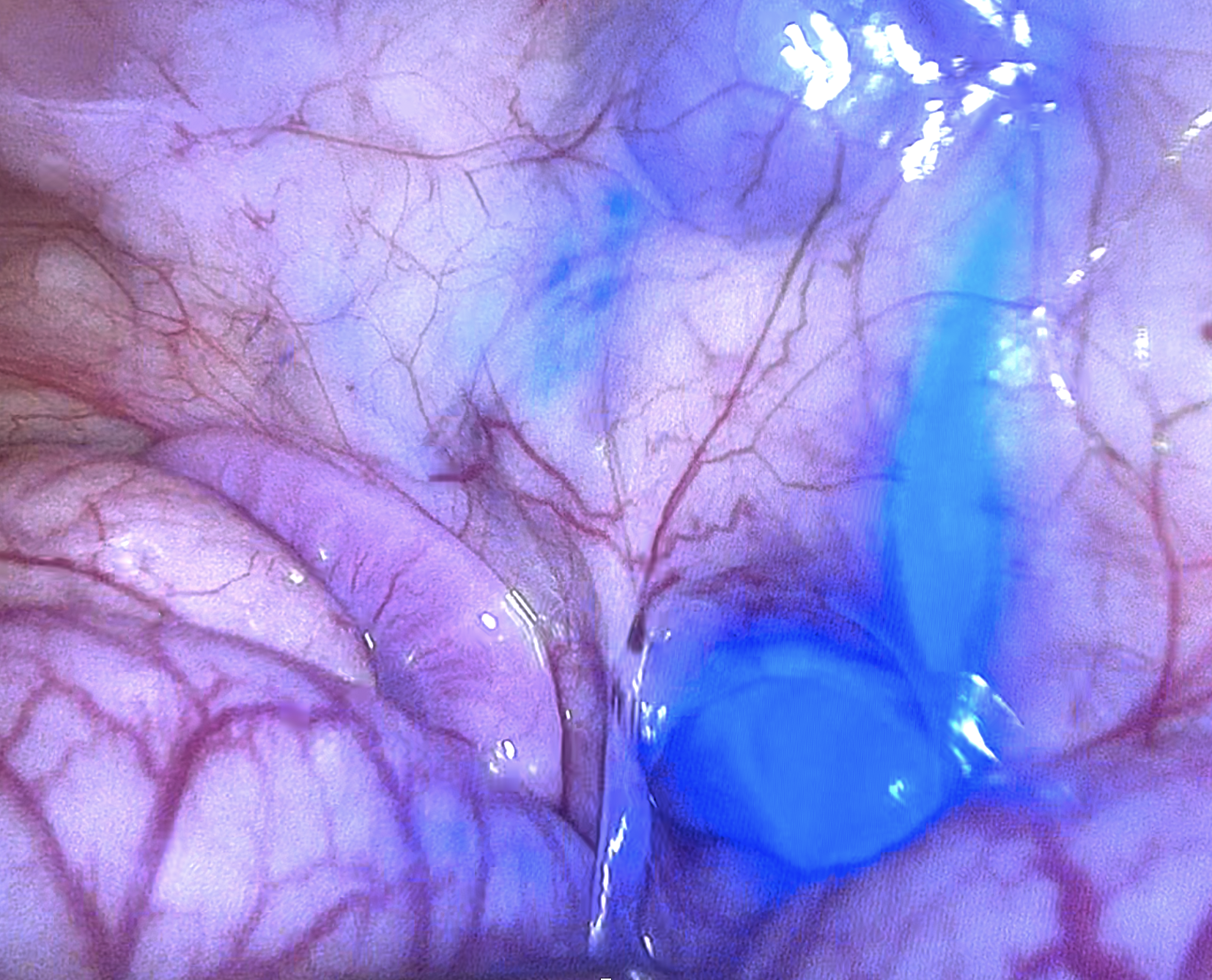
Les lambeaux cutanés, utilisés pour combler des pertes de substance après traumatisme ou exérèse tumorale, sont sujets à des complications liées à une mauvaise perfusion : ischémie, nécrose partielle ou totale. Grâce à l’angiographie par fluorescence, la viabilité du lambeau peut être évaluée objectivement avant sa transposition.
L’ICG permet de visualiser la microvascularisation cutanée en temps réel. Les zones bien perfusées apparaissent intensément fluorescentes, tandis que les régions à risque restent sombres. Cela aide le chirurgien à ajuster le design du lambeau, notamment pour les lambeaux axiaux, dont le succès repose sur la préservation de pédicules artériels spécifiques. Cette technique, bien que exigeante sur le plan de l’interprétation des images, s’avère précieuse pour améliorer les résultats esthétiques et fonctionnels.
Chylothorax : ligature du canal thoracique assistée par fluorescence
Le chylothorax idiopathique est une affection rare mais grave, nécessitant la ligature du canal thoracique pour stopper l’épanchement chyleux. Le défi principal réside dans l’identification peropératoire de ce canal, souvent enfoui dans la graisse médiastinale.
L’injection ciblée d’ICG (nœud poplité, coussinet métatarsien, ou mésentère) permet de visualiser avec un contraste élevé les structures lymphatiques afférentes. En thoracoscopie, la fluorescence offre une carte dynamique du canal thoracique et de ses branches accessoires, facilitant une ligature complète. Cette méthode permet d’atteindre un taux de résolution clinique de 85 à 95 %, tout en réduisant le traumatisme chirurgical et la durée d’hospitalisation.
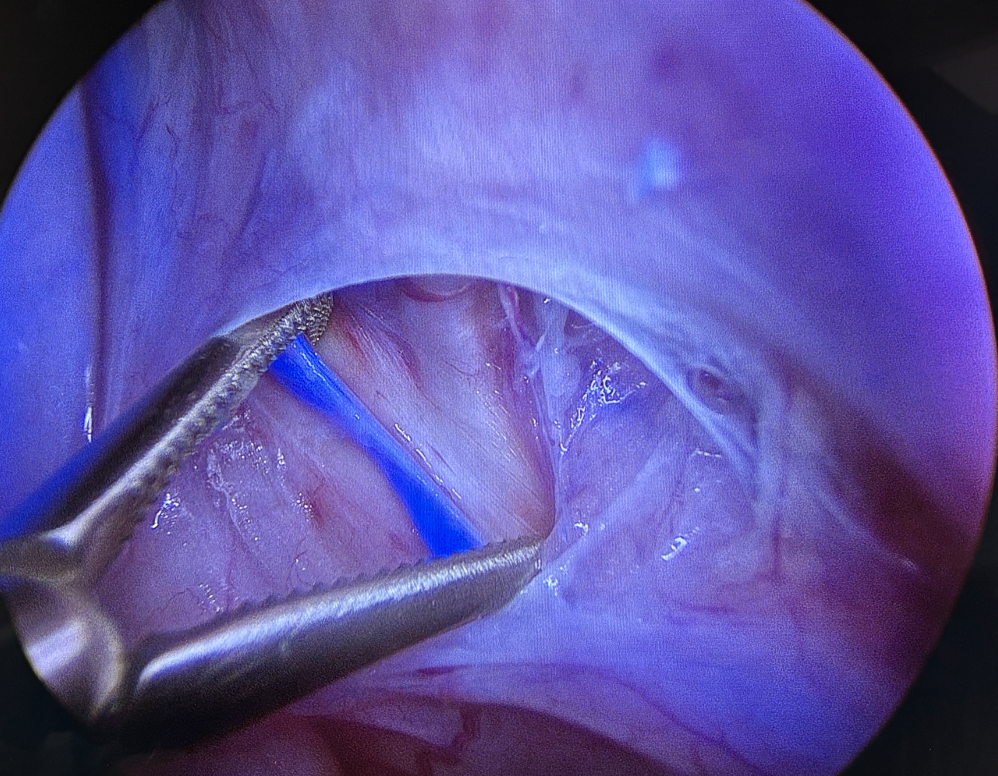
Visualisation du canal thoracique et de ses branches accessoires après injection d’ICG dans le nœud lymphatique mésentérique par thoracoscopie.
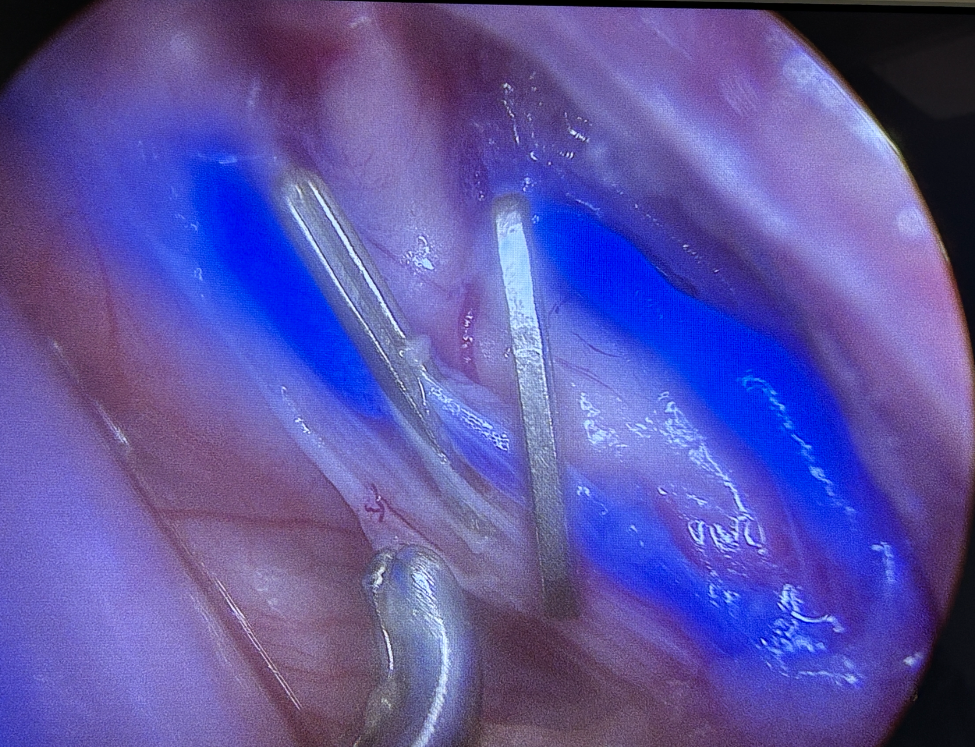
Mise en place de clip sur le canal thoracique par thoracoscopie.
Conclusion
La chirurgie guidée par fluorescence, en intégrant l’imagerie dynamique au geste chirurgical, marque une avancée décisive en médecine vétérinaire. Par son apport en visualisation tissulaire, elle permet une meilleure compréhension des structures anatomiques, réduit les complications peropératoires et améliore les résultats cliniques.
Déjà bien implantée en médecine humaine, cette technologie s’adapte progressivement aux réalités de la pratique vétérinaire, portée par une volonté d’innovation et de progrès thérapeutique. Son adoption plus large reste conditionnée par l’accessibilité des équipements, la formation des praticiens et l’optimisation des protocoles. Mais l’avenir de la chirurgie vétérinaire semble désormais éclairé — au sens propre — par la lumière de la fluorescence.